レブロジルⓇ概要
MDS患者における日常生活の負担

- EUMDS登録で新規に診断されたIPSSのLow又はIntermediate-1のMDS患者1985人が初診時に実施したEQ-5Dに基づく1)
- MDS患者358例を対象に実施されたインターネットを介した自己評価の調査結果のうち、輸血を受けていた234例の結果に基づく4)
EUMDS; European MDS Registry
- 1)Stauder R, et al.: Leukemia. 2018; 32: 1380-1392.
- 2)Ria R, et al.: Clin Interv Aging. 2009; 4: 413-423.
- 3)Soper J, et al.: Patient Relat Outcome Meas. 2022; 13: 31-38.
- 4) Sekeres MA, et al.: Oncologist. 2011; 16: 904-911.
- ⽂献1,3)の著者らは、Bristol-Myers Squibb又は⽶国Celgene Corporation(Bristol-Myers Squibbの関係会社)より
指導料などの謝⾦を受領したものを含む。
レブロジルⓇの概要
レブロジルⓇ皮下注用25mg・75mg(一般名:ルスパテルセプト、以下レブロジルⓇ)は、赤血球成熟促進薬であり、ヒトアクチビン受容体ⅡB型(ActRⅡB)の細胞外ドメインに免疫グロブリンG1(IgG1)-結晶化フラグメントドメインを結合した修飾体から構成される組換え融合タンパク質です。貧血治療薬として広く使われるエリスロポエチン製剤は初期赤血球前駆細胞の増殖及び分化を直接刺激するのに対し、レブロジルⓇは造血幹細胞から赤血球への分化過程の後期段階における分化を促進し、成熟した赤血球数の増加を誘導すると考えられています。
レブロジルⓇは、3つの臨床試験(COMMANDS試験、MEDALIST試験、MDS-003試験)により、赤血球輸血依存/非依存の低リスク骨髄異形成症候群(MDS)患者に対する有効性及び安全性が検討され、治療選択肢となることが示されたため、2024年1月に「骨髄異形成症候群に伴う貧血」に対して承認を取得しました。
レブロジルⓇの作用機序1-3)
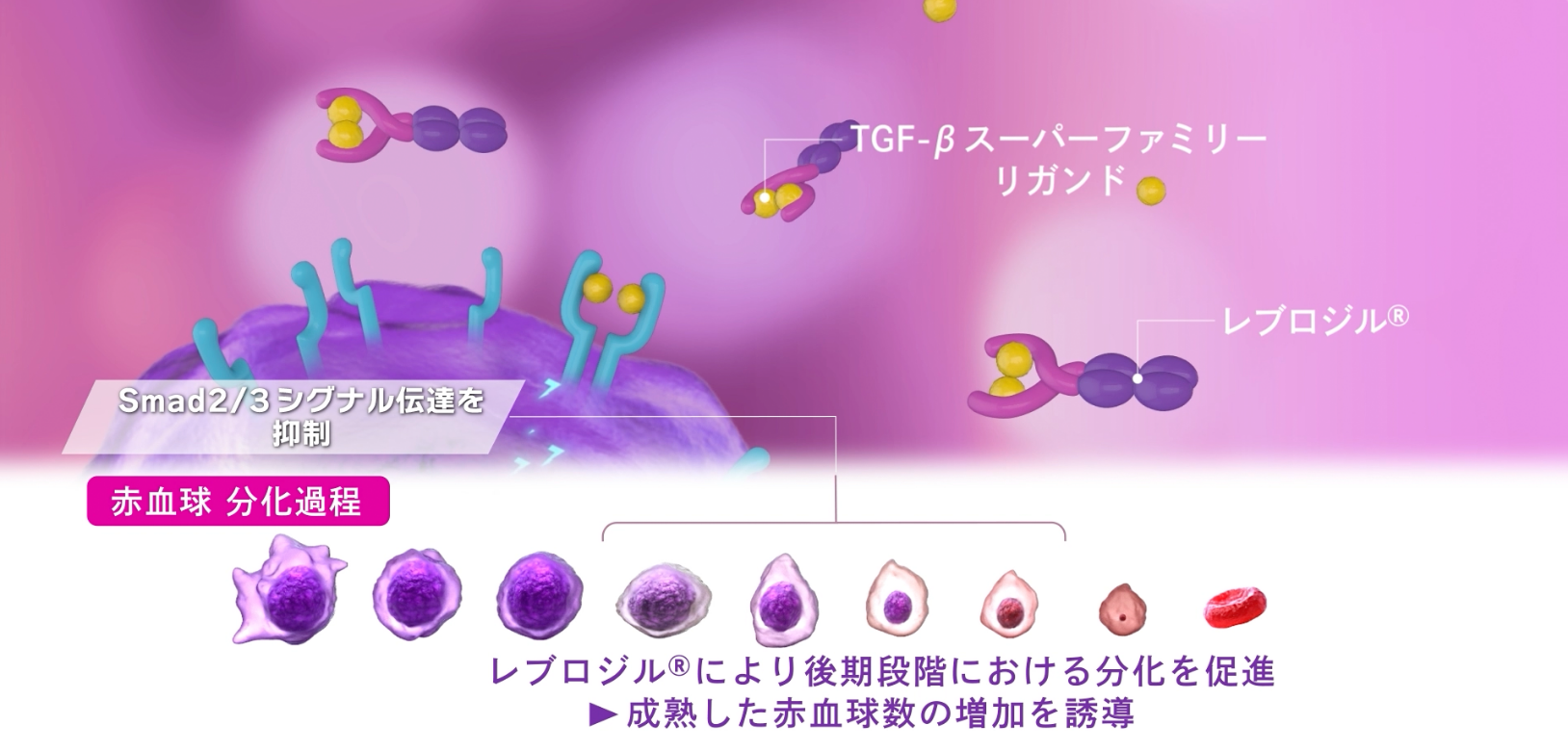
骨髄異形成症候群(MDS)に伴う貧血に対する赤血球成熟促進薬であるレブロジルⓇは、骨髄内の造血幹細胞から赤血球への分化過程の後期段階における分化を促進し、成熟した赤血球数の増加を誘導すると考えられています。
- 1)社内資料(承認時評価資料):薬理試験の概要文(2024年1月18日承認、CTD2.6.2.1)
- 2)Suragani RNVS, et al.: Nat Med. 2014; 20: 408-414.
- 3)Attie KM, et al.: Am J Hematol. 2014; 89: 766-770.
- 文献2,3)の著者らは、米国Celgene Corporation(Bristol-Myers Squibbの関係会社)の社員や指導料などの謝金を受領したものを含む。
レブロジルⓇの臨床試験
国際共同第Ⅲ相試験:COMMANDS試験
国際共同第Ⅲ相試験:COMMANDS試験において、赤血球輸血依存*1で、赤血球造血刺激因子製剤の治療歴がなく、環状鉄芽球陽性又は陰性を問わない、低リスク*2の骨髄異形成症候群*3(環状鉄芽球と血小板増加を伴う骨髄異形成/骨髄増殖性腫瘍を含む)患者を対象に、レブロジルⓇとエポエチン アルファ(遺伝子組換え)(本適応は国内未承認*4)の有効性を比較・検証、安全性を検討しました。
COMMANDS試験 
海外第Ⅲ相試験:MEDALIST試験
海外第Ⅲ相試験:MEDALIST試験において、赤血球輸血依存*5で、赤血球造血刺激因子製剤に対して不応、不耐容又は不適格で、環状鉄芽球陽性*6の低リスク*2骨髄異形成症候群*3[WHO分類改訂第4版(2017年)において定義される環状鉄芽球と血小板増加を伴う骨髄異形成/骨髄増殖性腫瘍に該当する患者を含む]患者を対象に、レブロジルⓇとプラセボの有効性を比較・検証、安全性を検討しました。
MEDALIST試験 
国内第Ⅱ相試験:ACE-536-MDS-003試験
国内第Ⅱ相試験:ACE-536-MDS-003試験において、赤血球輸血非依存*7で、環状鉄芽球陽性又は陰性を問わない、低リスク*2の骨髄異形成症候群の日本人患者を対象に、レブロジルⓇの有効性及び安全性を検討しました。
MDS-003試験 
- 無作為化前8週間の赤血球輸血量が2~6単位の患者を対象とした。なお、当該赤血球輸血は、赤血球輸血時又は輸血実施前7日以内のヘモグロビン濃度が9.0g/dL以下(貧血症状がある場合)又はヘモグロビン濃度が7.0g/dL以下(貧血症状がない場合)でなければならないとした。また、無作為化前の最後の赤血球輸血実施後のヘモグロビン濃度が11.0g/dL未満の患者を対象とした
- IPSS-Rによるリスク分類がVery low、Low又はIntermediate
- 5番染色体長腕部欠失を伴う骨髄異形成症候群患者は除外した
- エポエチン アルファは「骨髄異形成症候群に伴う貧血」の適応は国内未承認
- 無作為化前16週間において、①平均赤血球輸血量が8週間あたり2単位以上、②連続8週間無輸血の期間がないこと、及び③赤血球輸血前7日以内のヘモグロビン濃度が10.0g/dL以下を満たす患者を対象とした
- 骨髄中の環状鉄芽球が赤血球前駆細胞の15%以上(ただし、SF3B1遺伝子変異を有する場合は骨髄中の環状鉄芽球が赤血球前駆細胞の5%以上)の場合を環状鉄芽球陽性、それ以外の場合を環状鉄芽球陰性と定義した
- 組入れ前16週間に赤血球輸血を受けておらず、かつ組入れ前のヘモグロビン濃度(2回測定の平均値)が10.0g/dL未満の貧血症状を有する患者を対象とした
レブロジルⓇの用量調節
レブロジルⓇの
用量調節のポイント
再生時間|07:47
- レブロジルⓇは3週間に1回皮下投与する薬剤であり、同一用量を2回(6週間)以上連続投与した後に、十分なヘモグロビン濃度の上昇が認められない場合又は赤血球輸血から離脱できない場合には、2段階まで増量を検討することができます。
- ただし、赤血球輸血を受けていない状態で、ヘモグロビン濃度が3週間以内に2g/dLを超える急激な上昇が認められた場合や Grade 3以上の副作用が発現した場合は減量や休薬する必要があります。
用量調節 
4. 効能又は効果
骨髄異形成症候群に伴う貧血
5. 効能又は効果に関連する注意 (抜粋)
5.1 IPSS-R注)によるリスク分類のHigh及びVery Highに対する有効性及び安全性は確立していない。
注) Revised International Prognostic Scoring System(国際予後スコアリングシステム改訂版)
6. 用法及び用量
通常、成人にはルスパテルセプト(遺伝子組換え)として1回1.0mg/kgを3週間間隔で皮下投与する。なお、患者の状態により適宜増減するが、1回1.75mg/kgを超えないこと。
7. 用法及び用量に関連する注意
7.1 以下の基準を参考に、本剤を増量、休薬、減量又は中止すること。[8.2参照]
本剤の増量、休薬又は減量基準

注)GradeはNCI-CTCAE v4.03に準じる。
本剤の用量レベル
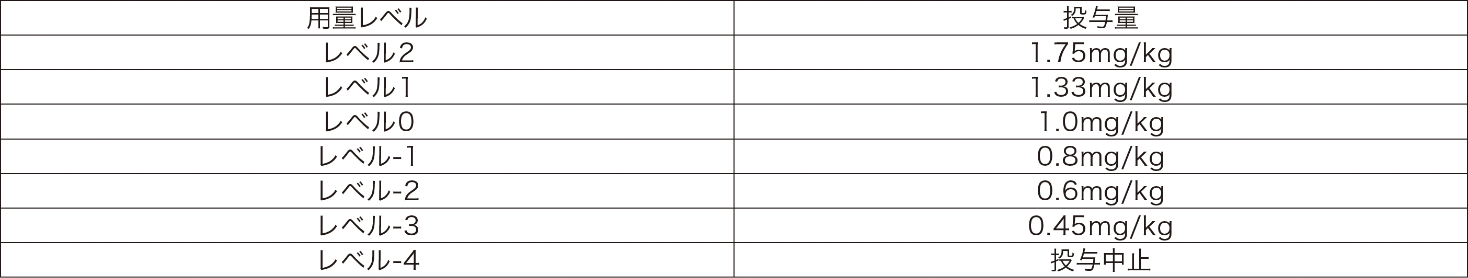
7.2 本剤1.75mg/kgを3回(9週間)投与した時点を目安として、輸血量の減少やヘモグロビン濃度の上昇等の効果が認められない場合には、本剤の投与継続の要否を検討すること。
8. 重要な基本的注意 (抜粋)
8.2 本剤投与中はヘモグロビン濃度を定期的に観察し、必要以上の造血作用があらわれないように十分注意すること。[7.1参照]